Was ist Phosphatdiabetes?
Letzte Aktualisierung: 17.07.2020
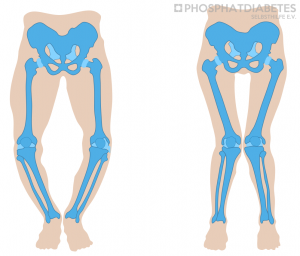 Die X-chromosomal-dominante hypophosphatämische Rachitis ist eine angeborene Störung, die neben dem Skelettsystem auch die Zähne in ihrer Mineralisation beeinflusst.
Die X-chromosomal-dominante hypophosphatämische Rachitis ist eine angeborene Störung, die neben dem Skelettsystem auch die Zähne in ihrer Mineralisation beeinflusst.
Die Erkrankung kann ab dem Ende des ersten Lebensjahres, meist mit dem eigentlichen Laufalter im zweiten Lebensalter, durch einen watschelnden, breitbeinigen Gang und einem verminderten Längenwachstum auffallen. Bei einzelnen Betroffenen kann die Diagnose auch erst im Schulalter aufgrund von Beinschmerzen und / oder einer zunehmenden Beinachsenfehlstellung (O- oder X-Beine) diagnostiziert werden.
Ursache der Erkrankung
Ein gesunder fester Knochen besteht aus einer Knochengrundsubstanz sowie aus einem bestimmten Verhältnis der Mineralien Calcium und Phosphat. Kommt es nun zu einer Störung einer dieser drei wichtigen Bestandteile, so kann es zu einer Weichheit des Knochens und damit besonders an den unteren Extremitäten zu einer Verbiegung der Unter- und/oder Unterschenkel oder auch zu einer Fraktur kommen.
Bei der oben genannten Form der hypophosphatämischen Rachitis (XLH) kommt es durch eine genetische Veränderung im sogenannten PHEX-Gen zur vermehrten Bildung des Hormons Fibroblast Growth Factor 23 (FGF23). FGF23 wird in den Knochenzellen gebildet und reguliert normalerweise neben dem Vitamin D den Phosphat-Haushalt des Körpers. Kommt es nun aber durch die genetische Veränderung zu einer vermehrten Bildung von FGF23, so führt dies zu einer vermehrten Ausscheidung von Phosphat über die Nieren. Normalerweise wird 90% des von der Niere filtrierten Phosphats in den Körper zurückgeführt. Durch die vermehrte FGF23-Konzentration kommt es aber zu einer Störung dieser Rückresorption und zu einer überproportional starken Ausscheidung von Phosphat über die Nieren in den Urin. Dieses führt im Blut zu einem niedrigen Phosphat-Spiegel und damit zu einer verminderten Konzentration von Phosphat im Skelettsystem. Darüber hinaus vermindert FGF23 die Synthese von aktivem Vitamin D in den Nieren. Durch den Phosphat-Mangel im Knochen und Mangel an aktivem Vitamin D kommt es zu einer Mineralisationsstörung und damit zu einer Weichheit des Knochens, die sich besonders in den Beinen darstellt und als hypophosphatämische (= zu wenig Phosphat) Rachitis bezeichnet wird.
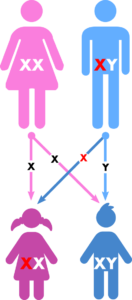
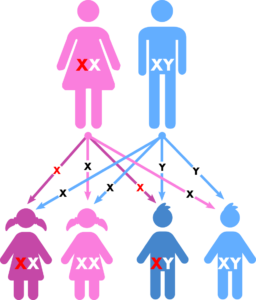
Die Erkrankung ist an das X-Chromosom gekoppelt. Das heißt, bei einer Erkrankung des Vaters sind alle Töchter betroffen und alle Söhne gesund, während statistisch die Hälfte der Söhne und die Hälfte der Töchter einer an Phosphatdiabetes erkrankten Mutter betroffen sein können. Die Ausprägung der Erkrankung ist durchaus auch innerhalb einer Familie sehr verschieden. Mittlerweile sind über 300 verschiedene krankheitsauslösende genetische Veränderungen im PHEX-Gen (Mutationen) beschrieben. Neben der vererbten Form eines Phosphatdiabetes gibt es Patienten aus Familien, in denen zuvor weder Vater noch Mutter an einem Phosphatdiabetes erkrankt waren. Dies ist etwa bei einem Drittel der Patienten der Fall. Man spricht dann von einer Spontan-Mutation.
Die Häufigkeit dieser seltenen Knochenerkrankung wird auf etwa ein betroffenes Neugeborenes auf 20.000 bis 25.000 Neugeborene beziffert. Trotz dieser Seltenheit ist es die häufigste angeborene Rachitis-Form.
Diagnose
Kommt es nach dem Beginn des freien Laufens im zweiten Lebensjahr zu einer zunehmenden Verbiegung der unteren Beine (O-Beine) oder möchte ein Kleinkind am Ende des zweiten Lebensjahres nicht gerne laufen, sollte der Kinderarzt eine Blutuntersuchung durchführen. In dieser Untersuchung ist zunächst ein Vitamin D-Mangel auszuschließen. Dieser kommt sehr viel häufiger als ein Phosphatdiabetes vor und kann ebenfalls Ursache einer O-Beinstellung im Kleinkindesalter sein. Haben aber die Eltern eine Vitamin D-Prophylaxe im ersten und zweiten Lebensjahr durchgeführt, so ist ein Vitamin D-Mangel als Ursache der O-Beine sehr unwahrscheinlich. Zeigt sich in der Blutabnahme ein erniedrigter Serum-Phosphat-Wert (<1 mmol/l) und ist der Marker für den Knochenumsatz erhöht (Alkalische Phosphatase), dann sollte eine Vorstellung des Kindes beim Spezialisten für Hormonstörungen (Kinderendokrinologie: www.dgked.de) oder beim Spezialist*innen für Nierenerkrankungen (Kindernephrologie: www.gpn.de) erfolgen.
Diese Spezialist*innen führen dann weitere Laboruntersuchungen durch, um die Verdachtsdiagnose Phosphatdiabetes zu bestätigen oder zu entkräften. Neben zusätzlichen Laborwerten ist auch eine Röntgenaufnahme zumeist der linken Hand erforderlich. In dieser Röntgenaufnahme könnte man dann bei Vorliegen eines Phosphatdiabetes sogenannte rachitische Veränderungen finden. Diese sind Hinweise auf eine gestörte Mineralisation des Knochens. Die Erkrankung kann bei ca. 80% der Patienten durch eine genetische Untersuchung weiter gesichert werden. Dies sollte bei negativer Familienanamnese oder unklaren Befunden angestrebt werden.
Bei Kindern mit von der Erkrankung betroffenen Eltern kann die Diagnose noch vor Manifestation von Symptomen bereits in den ersten Lebenswochen laborchemisch und/oder auch bei bekannter Mutation genetisch gestellt werden.
Therapie
Die Behandlung bei dieser Form der hypophosphatämischen Rachitis erfolgt entweder mit der „konventionellen“ medikamentösen Therapie bestehend aus mindestens 4 bis 6 über den Tag verteilten Gaben von Phosphat (zumeist als Lösung, bei älteren Kindern auch mittels Phosphatkapseln) in Kombination mit aktivem Vitamin D (Wirkstoff: Alfacalcidol oder Calcitriol) als Tropfen bzw. Tabletten. Es gibt alternativ dazu eine Antikörper-Therapie, die ab dem 2. Lebensjahr mit dem zugelassenen Medikament Burosumab (siehe unten) erfolgt.
Mit der Kombinationstherapie aus aktivem Vitamin D und Phosphat wird versucht, das über die Nahrung zugeführte Phosphat vermehrt über den Darm aufzunehmen und in den Körper einzuschleusen.
Im Idealfall gelingt es, so viel Phosphat ins Skelettsystem zu transportieren, dass sich die Aktivität des Knochenumsatz-Wertes (Alkalische Phosphatase im Serum) weitestgehend normalisiert, der Knochen gut mineralisiert und damit stabil und belastbar wird und sich das Wachstum verbessert. Je früher die Therapie eingeleitet wird, umso geringer ist das Risiko der Entstehung verstärkter Beinachsenfehlstellungen.
Leider kann es bei der Einnahme insbesondere des Phosphats zu Problemen kommen, denn das Phosphat schmeckt manchen Kindern nicht. Größere Gaben von Phosphat können zu Bauchschmerzen und Durchfall führen. Deshalb ist es wichtig, die tägliche Phosphatmenge auf möglichst viele kleine Portionen zu verteilen.
Seit Frühjahr 2018 steht für Phosphatdiabetes-Betroffene ab dem 2. Lebensjahr mit dem röntgenologischen Nachweis einer Knochenerkrankung eine zugelassene Therapie mit einem Antikörper zur Verfügung (Burosumab), der das erhöhte körpereigene FGF23 gezielt bindet und neutralisiert. Das Medikament mit dem Wirkstoff Burosumab wird alle 14 Tage unter die Haut gespritzt. Dies wird fachmännisch von einem Homecare-Service durchgeführt.
Unter der Therapie kommt es meist nach wenigen Injektionen zu einer Normalisierung der ursprünglich deutlich erhöhten Phosphatausscheidung über den Urin. Der Blut-Phosphatwert steigt in den unteren Normalwertbereich. Das Skelettsystem wird nun ausreichend mit Phosphat versorgt, die Skelettmineralisation verbessert sich zunehmend. Mittel- bis längerfristig zeigt sich im Röntgenbild eine deutliche Verbesserung der Knochenmineralisierung. Nach mehrjähriger Therapie sind auch Ausgradigungen der ursprünglichen Beinachsenfehlstellungen beobachtet worden. Dies kann jedoch auch unter der konventionellen Therapie beobachtet werden.
Nach Beginn der Therapie sind zunächst in den ersten Wochen kurzfristige Vorstellungen zur Kontrolle der Verträglichkeit, aber auch zur Dosisanpassung von Burosumab erforderlich. Dies wird mit Blut- und Urinkontrollen kontrolliert. Nicht selten ist eine Erhöhung der Medikamentendosis erforderlich.
Die Medikation wird in der Regel gut vertragen, schwere Nebenwirkungen wurden bisher nicht berichtet. Über evtl. entstehende langfristige Nebenwirkungen liegen noch keine Erkenntnisse vor, dies gilt es weiter zu beobachten.
Das Für und Wider der beiden Therapiemöglichkeiten ist ausführlich in einer europäischen Therapieempfehlung dargelegt worden (siehe unten).
Kontrolle der medikamentösen Einstellung
Nach Beginn der medikamentösen Therapie, unabhängig ob durch Phosphat- und Vit D Gaben oder durch Injektion des Antikörpers, ist zunächst alle 4 bis 6 Wochen, später dann alle 3 Monate, eine Vorstellung des Kindes bzw. Jugendlichen bei spezialisierten Medizinier*innen sinnvoll. Bei diesen Kontrollvorstellungen erfolgen dann Untersuchungen des Urins sowie des Blutes. Dort wird dann in Abhängigkeit von den Laborwerten möglicherweise eine Korrektur der bisherigen Medikation durchführen.
Empfohlene zusätzliche Untersuchungen
Nieren
Durch die medikamentöse Therapie mit Phosphat und aktiven Vitamin D kann es vereinzelt zu Kalkablagerungen in der Niere kommen (Nephrocalcinose). Es sollte deshalb etwa alle ein bis zwei Jahre eine Ultraschalluntersuchung der Nieren erfolgen.
Skelettsystem
Bei Betroffenen mit Phosphatdiabetes sind zumeist die Ober- und/oder Unterschenkel oft in starker X- oder O-Beinstellung gebogen. Dadurch kommt es zu einem auffälligen Gangbild. Je früher Diagnose gestellt und eine Behandlung begonnen wird, umso größer ist die Möglichkeit, dass sich diese Beinfehlstellung wieder unter alleiniger Medikation korrigiert. Sollte sich diese aber nach einer konsequent durchgeführten medikamentösen Therapie über 3 bis 4 Jahren nicht einstellen, so ist eine Wachstumslenkung mittels Epiphyseodese (z.B. sogenannter Eight-Plates) in Betracht zu ziehen. Bei älteren Kindern / Jugendlichen kann auch ein größerer chirurgischer Eingriff („Umstellungsosteotomie“) erforderlich sein.
Wachstum
Kinder mit Phosphatdiabetes sind bei Geburt in der Regel normal groß und schwer. Ab dem 2. Lebensjahr kommt es durch eine verlangsamte Wachstumsgeschwindigkeit zu einem schlechteren Körperlängenwachstum als man es bei der Größe der Eltern erwarten würde. Auch bei guter medikamentöser Einstellung und geraden Beinen sind Betroffene als Erwachsene meist nur grenzwertig normalwüchsig, können aber bei großen Eltern als Erwachsene durchaus normalwüchsig sein.
Zähne
Bei Phosphatdiabetes kann auch eine Störung der Zahnschmelz- und Dentinentwicklung der Milchzähne, aber auch der bleibenden Zähne vorliegen. Nicht selten werden Fisteln, entzündliche Veränderungen der Zahnwurzelspitzen mit Vereiterungen (Abszesse) bei einem karies-freien Gebiss beobachtet. Um möglichen Zahnverlusten entgegenzuwirken, sind regelmäßige zahnärztliche Untersuchungen sinnvoll. In allererster Linie kommt es aber auf eine gründliche tägliche Zahnpflege und regelmäßige Prophylaxe-Maßnahmen an.
Gehör
Sehr selten kommt es im Verlauf zu einer Hörstörung im Innenohr. Sollten sich Hinweise auf eine Hörstörung ergeben, so ist eine Abklärung durch einen Hals-Nasen-Ohren-Arzt sinnvoll.
Kopfentwicklung
Sehr selten kommt es im Säuglings- und Kleinkindesalter zu einer auffälligen Entwicklung des Schädels (Kraniosynostose). Dann sollte mit Fachpersonen der Pädiatrie über eine Vorstellung in der Kinder-Neurochirurgie gesprochen werden.
Ausblick
Erweiterung des Behandlungsalters für die Burosumab-Therapie:
2020 wurde eine Phase 2 Studie für die Behandlung mit Burosumab vom Kleinkindalter bis in die Adoleszenz für das Säuglingsalter begonnen an der auch 3 deutsche Zentren teilnehmen.
Am 2.Oktober 2020 erhielt Burosumab durch die Europäische Kommission eine Zulassungserweiterung für die Behandlung von älteren Jugendlichen sowie Erwachsenen mit X-chromosomaler hypophosphatämischer Rachitis (XLH).
Dadurch ist diese Behandlung nun auch für Jugendliche mit radiologischem Nachweis der Knochenerkrankung unabhängig vom Wachstumsstatus möglich.
Europäische Therapieempfehlungen
Im Dezember 2017 hat sich eine Gruppe von 20 Fachpersonen aus dem Bereich Kinderheilkunde, Nephrologie, Endokrinologie, Orthopädie, Zahnheilkunde und Neurochirurgie, sowie Vorstandsmitgliedern der Organisation Phosphatdiabetes e.V. aus Deutschland und der entsprechenden Organisation aus Frankreich in Berlin getroffen, um Therapieempfehlungen für diese seltene Erkrankung zu erarbeiten. Diese sind seit Juli 2019 in einer sehr renommierten Fachzeitschrift publiziert (Haffner et al Nat Rev Nephrol 2019) und können kostenlos als open access publication eingesehen werden (https://doi.org/10.1038/s41581-019-0152-5). An einer deutschsprachigen Übersetzung wird gerade gearbeitet.
Patient*innenregister
Um mehr über den Krankheitsverlauf und die Effektivität der Therapie des Phosphatdiabetes bei Kindern und Jugendlichen zu erfahren, haben sich Fachleute der Kinderendokrinologie und Kindernephrologie aus Deutschland zusammengeschlossen, um ein Patient*innenregister zu initiieren. Hierbei werden nach entsprechender Aufklärung und schriftlicher Einverständniserklärung der Eltern und Patient*innen die relevanten klinischen Daten der Patient*innen nach entsprechender Unkenntlichmachung der persönlichen Daten („Pseudonymisierung“) in eine Datenbank eingegeben. Unterdessen konnten bereits 20 Behandlungszentren mit mehr als 50 Patient*innen in das Register eingeschlossen werden. Geplant ist der Einschluss von 150 Patient*innen aus 39 Zentren. Die Teilnehmenden des Studienregisters treffen sich einmal pro Jahr. Im Rahmen des Registers sind auch weitere klinische Studien zur Behandlung der Erkrankung vorgesehen.
Zusätzlich sollen, z.B. über die ERNs (Europäische Referenznetzwerke), auch für erwachsene XLH-Patient*innen Register initiiert werden.
Resümee
XLH ist eine seltene angeborene Erkrankung, die im Wesentlichen das Skelettsystem und die Zähne der Erkrankten betrifft. Eine frühzeitige Diagnose und Behandlung ist notwendig, um Komplikationen, insbesondere am Skelettsystem aber auch anderen Organen, zu verhindern. Durch die Entwicklung und Zulassung von Burosumab sind die Möglichkeiten der medikamentösen Therapie wesentlich erweitert worden. Erstmals sind bei den Behandelten normale Phosphatkonzentrationen im Blut nachweisbar, die nach ca. 9 bis 12 Monaten zu einer deutlichen Besserung der Knochenmineralisierung führen. Wegen der Beteiligung verschiedener Organe bei der Erkrankung sollte möglichst die Betreuung durch ein multidisziplinäres Team in einer Spezialsprechstunde erfolgen.
Literatur
Haffner D, Emma F, Eastwood D, Biosse Duplan M, Bacchetta J, Schnabel D, Wicart P, Bockenhauer D, Santos F, Levtchenko E, Harvent P, Kirchhoff M, Di Rocco, F Chaussain C, Brandi LM, Savendahl L, Briot K, Kamenicky P, Rejnmark L, Linglart A. Clinical practice recommendations for the diagnosis and management of X‑linked hypophosphatemia. Nat Rev Nephrol. 2019 Jul;15(7):435-455
Linglart A, Biosse-Duplan M, Briot K, Chaussain C, Esterle L, Guillaume-Czitrom S, Kamenicky P, Nevoux J, Prié D, Rothenbuhler A, Wicart P, Harvengt P. Therapeutic management of hypophosphatemic rickets from infancy to adulthood. Endocr Connect. 2014 Mar 14;3(1):R13-30
Rothenbuhler A, Schnabel D, Högler W, Linglart A. Diagnosis, treatment-monitoring and follow-up of children and adolescents with X-linked hypophosphatemia (XLH). Metabolism. 2020 Feb;103S:153892
Schnabel D, Hiort O. Endokrine Störungen des Mineralhaushaltes bei Kindern und Jugendlichen, in: Hiort O, Danne T, Wabitsch M (Hrsg.) Pädiatrische Endokrinologie und Diabetologie, 2. Auflage: 475-498, Springer Verlag, Berlin 2019
| Dr. med. Dirk Schnabel, Ltd. Oberarzt Stellv. Leiter SPZ für chronisch kranke Kinder Leitung, Abt. Interdisziplinär Pädiatrische Endokrinologie und Diabetologie Augustenburger Platz 1, (Mittelallee 7a) D 13353 Berlin E-Mail: dirk.schnabel@charite.de |
Prof. Dr. med. Dieter Haffner Klinik für Pädiatrische Nieren-, Leber- und Stoffwechselerkrankungen Zentrum für Kinderheilkunde und Jugendmedizin Medizinische Hochschule Hannover Carl-Neuberg Str.1 D 306325 Hannover E-Mail: haffner.dieter@mh-hannover.de |